Endoskopiskas retrogrādas holangiopankreatogrāfijas izraisītas agrīnās komplikācijas, riska faktori un pankreatīta profilakses iespējas
Kopsavilkums
Endoskopiska retrogrāda holangiopankreatogrāfija (ERHP) ir viena no biežākajām un informatīvākajām metodēm kopējā žultsvada patoloģijas gadījumā. Šo metodi lieto žultsvadu patoloģiju diagnostikai un ārstēšanai. Latvijā katru gadu tiek veiktas vairāk nekā 500 ERHP procedūras. Ir svarīgi apzināt procedūras indikācijas, potenciālos riska faktorus un komplikācijas, kā arī ieguvumus un metodes alternatīvas. Šajā pētījumā tika analizēta ERHP izraisītu agrīno komplikāciju izplatība, riska faktori un pankreatīta profilakses iespējas Paula Stradiņa Klīniskajā universitātes slimnīcā.
Pētījums ir prospektīvs, informācija iegūta, izmantojot stacionāra pacientu medicīnisko karšu datus par laikposmu no 2013. gada novembra līdz 2014. gada aprīlim. Tika analizēti 156 slimnieku ārstēšanas rezultāti. Pētījumā iekļautas 95 (60,9 %) sievietes un 61 (39,1 %) vīrietis. No visām procedūrām 75 % (n = 117) gadījumu ERHP tika veikta pirmo reizi, atkārtotas procedūras veiktas 25 % (n = 24) gadījumu. Veiksmīga kopējā žultsvada kanulācija tika novērota 90 % (n = 140) pacientu.
Biežākais iemesls neveiksmīgai kanulācijai bija endoskopiska asiņošana pre cut papillotomijas gadījumā (n = 5/16). Pēc ERHP manipulācijas agrīnās komplikācijas radās sešos gadījumos (9,36 %). Akūts pankreatīts bija biežākā agrīnā ERHP komplikācija – 4/156 (2,56 %), mirstība ir 1,56 %. Agrīnu komplikāciju attīstības riska faktori ietver ar pacientiem saistītus faktorus (vecums < 65 gadi, normāls bilirubīna līmenis serumā (p < 0,001)) un ar procedūru saistīto risku (ķirurģiska iejaukšanās ductus pancreaticus (p < 0,001)).
Pētījuma gaitā ir pierādīts, ka farmakoloģiskais aģents Supp. Diclofenac natrium 100 mg samazina agrīnu komplikāciju izplatības biežumu pēc ERHP manipulācijas (p < 0,045). ERHP ir droša un efektīva metode ar zemu komplikāciju risku. Visefektīvākā metode komplikāciju skaita samazināšanai pēc ERHP ir rūpīga pacientu atlase un riska faktoru analīze pirms procedūras.
Ievads
Endoskopiska retrogrāda holangiopankreatogrāfija (ERHP) ir metode, kas ietver divu metožu – endoskopijas un rentgena tehnoloģiju – vienlaicīgu pielietojumu. Pateicoties jauno tehnoloģiju attīstībai, metode ir efektīva žultsakmeņu, žultsvada striktūru, aizkuņģa dziedzera un aknu slimību endoskopiskai terapijai. Šādu manipulāciju 1968. gadā pirmo reizi veica Makkjūns (McCune) [12, 233]. Pēc pieciem gadiem šo metodi sāka lietot klīniskajā praksē daudzās pasaules valstīs [11, 75].
Līdz šim brīdim Latvijā ir veikti vairāki desmiti tūkstoši ERHP manipulāciju. Kaut gan veikto ERHP skaits ir samērā liels, komplikāciju risks joprojām ir salīdzinoši augsts (pat līdz 12 %) [5, 12], kas arī palielina mirstību. Laika gaitā, palielinoties klīniskajam materiālam, uzlabojoties manipulācijas tehnikai, mainījās arī ERHP indikācijas un kontrindikācijas. Darba autori uzskata, ka ir jāpārskata ERHP ārstēšanas rezultāti, komplikāciju mazināšanas pasākumi un pacienta pēcoperācijas aprūpes īpatnības.
Darba mērķis
Balstoties uz pētījuma rezultātiem un literatūras datiem, izvērtēt endoskopiskas retrogrādas holangiopankreatogrāfijas agrīnās komplikācijas, epidemioloģiskos datus un riska faktorus un to profilakses iespējas, lai mazinātu ar ERHP asociēto komplikāciju biežumu un tādējādi arī mirstību.
Materiāls un metodes
Pētījuma dizains – prospektīvs pētījums.
Pētījuma dizains – prospektīvs pētījums. Informācija iegūta, izmantojot stacionāra pacientu medicīnisko karšu datus par laikposmu no 2013. gada novembra līdz 2014. gada aprīlim. Pētījumā tika iekļauti P. Stradiņa Klīniskās universitātes slimnīcas pacienti, kuri atbilda visiem kritērijiem un kuriem nebija neviena izslēgšanas kritērija. Pirms izmeklēšanas visi pacienti parakstījās, ka piekrīt dalībai pētījumā.
Iekļaušanas kritēriji:
- abu dzimumu ambulatorie vai stacionāra pacienti;
- pacientam veikta pirmreizēja vai atkārtota ERHP.
Izslēgšanas kritēriji:
- pacientam ir kontrindicēta ERHP;
- pacientam ir veikta cita invazīva manipulācija žultsvados (transkutāna holangiopankreatogrāfija (TPHA), ķirurģiska anastomoze).
Visiem pacientiem pirms procedūras tika veiktas:
- bioķīmiskās analīzes, lai noteiktu fermentu, kas sintezējas aknu šūnās (ALAT, ASAT), aktivitāti, bilirubīna, sārmainās fosfatāzes līmeni serumā. Visiem pacientiem tika noteikts seruma lipāzes līmenis pirms procedūras un 12–16 stundas pēc procedūras;
- radiodiagnostiskie izmeklējumi (vēdera dobuma ultrasonogrāfija (US), datortomogrāfija (DT) vai magnētiskā rezonanse (MR) vēdera dobuma orgāniem), lai izvērtētu kopējā žultsvada stāvokli – diametru, žultsakmeņu klātbūtni, mehāniskās dzeltes cēloni.
Visi pacienti tika novēroti stacionārā vismaz 24 stundas pēc procedūras.
ERHP indikācijas un kontrindikācijas bija vispāratzītās [5, 12]. Atkārtota ERHP procedūra tiek veikta šādos gadījumos: kopējā žultsvada stenta maiņa, holedoholitiāzes recidīvs. ERHP procedūras veica trīs endoskopisti; diviem no tiem pieredze ERHP jomā – vairāk nekā 500 procedūru, vienam – mazāk nekā 50 procedūru.
Klīniskajā praksē kopējā žultsvada patoloģijas gadījumā gan diagnostiskos, gan terapeitiskos nolūkos arvien plašāk lieto endoskopisko retrogrādo holangiopankreatogrāfiju. Terapeitiskās ERHP gadījumā pārsvarā izmanto papillotomiju kā tehniku selektīvai kopējā žultsvada kanulācijai, kas ir veiksmīga 80–95 % gadījumu. Dziļo kanulāciju, kad katetra uzgalis šķērso papilla duodeni major, veic, lai ievadītu kontrastvielu, vizualizētu maģistrālos žultsvadus un izdarītu nepieciešamās terapeitiskās procedūras. Dziļā kopējā žultsvada kanulācija neizdodas (ap 5 %), ja žultsvada atvere ir lokalizēta vairāk distāli, akmeņi cieši saspiež ampulla hepatopancreatica un ir papillas tūska. Šādos gadījumos veic pre-cut sfinkterotomiju, izmantojot adatas nazi. Pre-cut sfinkterotomija ir indicēta pacientiem ar apgrūtinātu kopējā žultsvada kanulāciju, lai piekļūtu žultsvadiem. Pēc sfinkterotomijas ir iespējams papildus veikt visas nepieciešamās terapeitiskās manipulācijas, piemēram, izvilkt akmeņus, ievietot stentu (endoprotēzi) [10, 52].
Agrīnās ERHP komplikācijas bija vispāratzītās [1, 468]:
- Pankreatīts (pankreatīta diagnoze tika noteikta, ja bija pozitīvi vismaz divi kritēriji):
1) augsts (vismaz 3 reizes augstāks par normu: 40–125 SV/l) lipāzes līmenis serumā nākamajā dienā;
2) sāpes vēderā 24 stundu laikā pēc procedūras;
aizkuņģa dziedzera tūska ar vai bez šķidruma kolekcijas ultrasonogrāfijas / datortomogrāfijas izmeklējumā nākamajā dienā. - Asiņošana – hemoglobīna līmeņa samazināšanas nākamajā dienā par vismaz 3 g/l.
- Perforācija – ar vizuālās diagnostikas (vēdera dobuma ultrasonogrāfija, datortomogrāfija vēdera dobuma orgāniem) metodes palīdzību vērojama šķidruma kolekcija.
- Infekcija – febrila temperatūra 24 stundas pēc manipulācijas.
- Kardiopulmonālās komplikācijas (sirds aritmija, hipoksija, aspirācija, troponīna I līmeņa paaugstināšanās).
Šajā pētījumā tika analizēti ERHP agrīno komplikāciju riska faktori. Tie tika iedalīti trīs grupās [4, 20]:
- ar pacientu saistītie faktori (demogrāfiskie dati, anamnēzes dati);
- ar procedūru saistītie faktori (manipulācijas veidi, terapijas dati);
- ar operatoru saistītais faktors (iepriekšējā pieredze: < 200 procedūru un > 200 procedūru).
Lai definētu kanulācijas sarežģītības pakāpi, pētījumā tika izmantota Skandināvijas kanulācijas definīcija 5 : 5 : 2 (5 minūtes : 5 mēģinājumi : 2 iejaukšanās d. pancreaticus) [7, 247].
Lai izvērtētu Diclofenac 100 mg kā profilaktisku pasākumu pēc ERHP izraisīta pankreatīta (PEP), visi pacienti pēc nejaušināšanas principa tika iedalīti divās grupās. Vienai pacientu grupai pēc procedūras PEP profilaksei rektāli tika ievadīts Supp. Diclofenac 100 mg (2 gab.), otrai pacientu grupai Supp. Diclofenac 100 mg (2 gab.) PEP profilaksei netika ievadīts. Supp. Diclofenac 100 mg tika pasūtīts slimnīcas aptiekā (ražotājs nebija svarīgs).
Katram pacientam tika aizpildīta oriģinālā anketa ar 24 parametriem, kurā tika iekļauti pacienta demogrāfiskie dati un sūdzības, ERHP indikācijas, lietotās manipulācijas metode un veids, procedūras komplikācijas un ERHP iznākums. Uz anketas pamata tika izveidota pacientu datubāze, izmantojot Microsoft Office Excel 2011 programmatūru. Statistiskie dati tika apstrādāti ar IBM SPSS Statistics Base Grad Pack 22.0 programmu. Darbā izmantoti medicīniskajos pētījumos vispāratzītie statistikas parametri: 1) centrālās tendences (vidējie aritmētiskie lielumi u. c.); 2) datu izkliedi raksturojoši lielumi (standartnovirze u. c.). Jebkuras p vērtības ir divpusējas un atbilst 5 % ticamībai. Visos gadījumos kritērijs būtiskuma līmenim, kurā noraidīja nulles hipotēzi, bija p ≤ 0,05.
Lai novērtētu vidējo vērtību atšķirības ticamību divās savstarpēji neatkarīgās grupās, tika izmantota neatkarīgu izlašu t-testa analīze. Savukārt, lai novērtētu pacientu skaita iedalījuma atšķirību divās dažādās grupās, tika izmantota Pīrsona hī kvadrāta (χ2) analīze un ticamības intervālu analīze.
Rezultāti
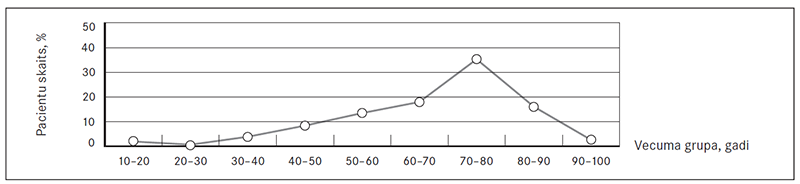
Pētījumā tika iekļauti 156 pacienti: 95 (61 %) sievietes un 61 (39 %) vīrietis. Jaunākajam pacientam bija 14 gadi, vecākajam – 91 gads. Vidējais vecums – 52,5 ± 38 gadi (sk. 1. att.).
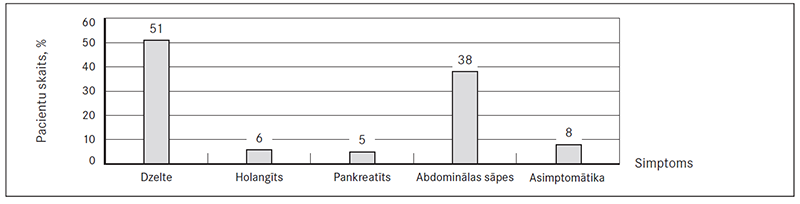
Biežākais simptoms pacientiem bija mehāniskā dzelte (51 %), nākamais – abdominālas sāpes (38 %), holangīts (6 %), pankreatīts (5 %), savukārt asimptomātika tika novērota 8 % pacientu (sk. 2. att.).
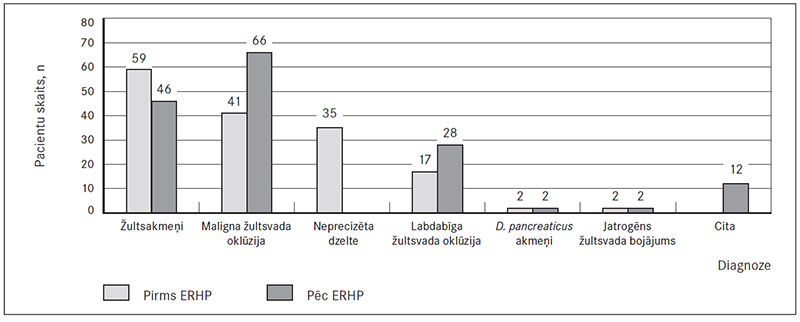
Visbiežākā indikācija ERHP veikšanai bija žultsakmeņi (38 %), nākamā – žultsvada maligna oklūzija (26 %), žultsvada labdabīga oklūzija (11 %) u. c. (sk. 3. att.). 75 % (n = 117) gadījumu procedūra tika veikta pirmreizēji, atkārtota procedūra veikta 25 % (n = 24) gadījumu, vidēji 4,5 mēnešus pēc iepriekšējās procedūras (minim. = 21 diena, maks. = 5 gadi).
Veiksmīga kopējā žultsvada kanulācija tika veikta 90 % (n = 140) slimnieku. Biežākais iemesls neveiksmīgai kanulācijai bija endoskopiska asiņošana pre cut papillotomijas gadījumā 31 % (n = 5/16). Žultsvada kanulācijas sarežģītības pakāpe visbiežāk bija zema (67 % jeb n = 94). Vidēja tika konstatēta 17 % (n = 24) gadījumu un augsta – 8 % (n = 12) gadījumu.
Sarežģītas pakāpes kanulācija visbiežāk tika saistīta ar anatomisku anomāliju, ierobežotu vizualizāciju un individuālu endoskopista pieredzi – ārstiem bija grūti (nav vienota standarta) noteikt kanulācijas pakāpi.
Papillotomija bija biežākā terapeitiskā procedūra. No visiem 122 pacientiem, kam tika veikta kopēja žultsvada kanulācija, papillotomija ar papillotomu tika veikta 108 (88,6 %) pacientiem un pre cut papillotomija – 14 (11,4 %) slimniekiem. No 117 (veiksmīga papillotomija) pacientiem 40 (34,2 %) pacientiem tika veikta papillotomija, 29 (25 %) – papillotomija ar žultsakmeņu balona ekstrakciju, 10 (8,5 %) – papillotomija ar žultsakmeņu groziņa ekstrakciju, 7 (6 %) – papillotomija ar balona ekstrakciju un groziņa ekstrakciju, 26 (22,1 %) – papillotomija ar žultsvada stenta implantāciju, 2 (1,7 %) – papillotomija ar d. pancreaticus akmeņu balona ekstrakciju un 3 (2,5 %) – papillotomija ar d. pancreaticus stenta implantāciju.
Visbiežāk procedūras laikā tika diagnosticēti žultsakmeņi (30 %), aizkuņģa dziedzera audzējs (28 %), papillīts (18 %), Papilla Vateri adenokarcinoma (8 %), holangiokarcinoma (6 %) un citas diagnozes – jatrogēns kopējā žultsvada bojājums, hronisks pankreatīts, ehinokokoze (10 %), kas vairumā gadījumu saskanēja ar nosūtīšanas diagnozēm (sk. 3. att.).
Agrīnas komplikācijas pēc ERHP konstatētas 9,36 % (n = 6/156) no visiem analizētajiem pacientiem. Biežākā komplikācija bija pankreatīts (2,56 % jeb 4/156), no tā nomira viens pacients. Vienam pacientam konstatēts holangīts un vienam pacientam – miokarda infarkts.
Lai izvērtētu agrīno komplikāciju riska faktorus, pacienti tika iedalīti trīs grupās: ar pacientiem saistītie faktori, ar procedūru saistītie faktori un ar operatoru saistītais faktors (sk. 1. tab.).
1. attēls. Pētījumā iekļauto pacientu iedalījums pa vecuma grupām / Patients included in research devided by age groups
2. attēls. Pētījumā iekļauto pacientu iedalījums pēc simptomātikas / Patients included in research devided by symptomatology
No visiem izvērtētiem faktoriem tika atrasta statistiski ticama pozitīva korelācija starp agrīno ERHP komplikāciju un pacienta vecumu (> 65 gadi), normālu bilirubīna līmeni serumā un ķirurģisku iejaukšanos d. pancreaticus, p < 0,0001. Pacientu dzimums statistiski ticami neietekmēja iegūtos rezultātus.
3. attēls. Pētījumā iekļauto pacientu diagnoze pirms un pēc endoskopiskas retrogrādas holangiopankreatogrāfijas (ERHP) / Patients included in research divided by diagnosis before and after ERCP
1. tabula. Agrīno komplikāciju riska faktoru analīze / Analysis of short-term complication risk factors
| Riska faktori | PEP / pacientu skaits, n | p vērtība | |
|---|---|---|---|
| Ar pacientiem saistītie riska faktori | Dzimums (sieviešu) | 2/95 | 0,064 |
| Vecums (< 65 gadi) | 3/94 | < 0,0001 | |
| Pankreatīts pēc iepriekšējās procedūras | 0/12 | 0 | |
| Normāls bilirubīna līmenis | 3/29 | < 0,0001 | |
| Normāls kopējā žultsvada diametrs | 1/25 | 0,083 | |
| Žultsakmeņi | 0/46 | 0 | |
| Aizkuņģa dziedzera audzējs | 0/44 | 0 | |
| Ar procedūru saistītie riska faktori | Pre cut papillotomija | 0/14 | 0 |
| Sarežģīta kanulācija | 0/12 | 0,076 | |
| Periampulārais divertikuls | 0/4 | 0 | |
| Žultsakmeņu evakuācija | 0/46 | 0 | |
| Kopējā žultsvada stentēšana | 1/26 | 0,076 | |
| D. pancreaticus akmeņu evakuācija | 0/3 | 0 | |
| Ķirurģiska iejaukšanās d. pancreaticus | 3/5 | < 0,0001 | |
| Ar operatoru saistītais risks faktors | > 200 procedūru | 3/114 | 0,038 |
| < 200 procedūru | 1/38 | 0,038 | |
| Pankreatīta profilakses efektivitātes izvērtēšana | I grupa (Supp. Diclofenac natrium 100 mg 2 gab. tika ievadīts) | 2/70 | 0,045 |
| II grupa (Supp. Diclofenac natrium 100 mg 2 gab. netika ievadīts) | 2/86 | 0,045 | |
PEP – pēc endoskopiskas retrogrādas holangiopankreatogrāfijas izveidojies pankreatīts.
Pacientiem, kas lietoja Supp. Diclofenac 100 mg pēc ERHP manipulācijas, PEP incidence bija 1,79 % gadījumu, salīdzinot ar pacientiem, kas nelietoja Supp. Diclofenac 100 mg pēc ERHP manipulācijas. Pēdējiem PEP incidence bija 2,21 % (p = 0,045) gadījumu.
Diskusija
ERHP ir manipulācija, ar kuru ikdienā saskaras daudzu specialitāšu ārsti (gastroenterologi, endoskopisti, ķirurģi u. c.), tāpēc ir svarīgi pārzināt šīs metodes absolūtās un relatīvās indikācijas un iespējamos riskus.
Pētījumā pacientu iedalījums pēc dzimuma (95 (61 %) sievietes un 61 (39 %) vīrietis) nebija viendabīgs, taču statistiski ticami neietekmēja iegūtos rezultātus. Šādu neviendabīgu iedalījumu varētu izskaidrot ar to, ka kopējā žultsvada patoloģija biežāk tiek diagnosticēta sievietēm, žultsakmeņu attīstības risks sievietēm ir trīs reizes lielāks (ģenētiska predispozīcija, grūtniecības, diētas un citi faktori) [5, 15].
Jaunākajam pacientam bija 14 gadi, vecākajam – 91 gads. Visbiežāk pacienti bija vecumā no 70 līdz 80 (n = 55/156) gadiem. Pētījuma dati liecina, ka manipulācija tiek lietota ļoti plašai vecuma grupai, turklāt tā biežāk ir nepieciešama vecāka gadagājuma pacientiem (dati līdzinās citu gastroenteroloģijas klīniku rezultātiem). Vēl jo vairāk – gados veciem pacientiem ir daudz blakusslimību, kas palielina ERHP komplikāciju risku [13, 849].
Saskaņā ar pētījuma datiem visbiežākā manipulācijas indikācija bija mehāniskā dzelte, kas korelē ar literatūras datiem. ERHP manipulācija ir labāka izvēle etioloģijas precizēšanai un ārstēšanai šīs patoloģijas gadījumā [1, 470].
Biežākā pirmsprocedūras diagnoze bija žultsakmeņi kopējā žultsvadā, kā nākamās – labdabīgas un ļaundabīgas kopējā žultsvada oklūzijas. Tas atbilst arī literatūras datiem. Respektīvi, ERHP, salīdzinot ar citām metodēm, ir priekšroka pacientiem ar šādām diagnozēm, lai veiktu žultsakmeņu evakuāciju, precizētu oklūzijas cēloni, implantētu stentu kopējā žultsvadā [1, 471].
Veiksmīga kopējā žultsvada kanulācija tika veikta 90 % (n = 140) slimnieku. Pēdējais pētījums par kanulācijas efektivitāti P. Stradiņa Klīniskajā universitātes slimnīcā (PSKUS) tika veikts 2008. gadā, un dati liecina, ka kanulācijas efektivitāte pa šo laiku uzlabojusies par 2 %. To varētu skaidrot ar endoskopistu kvalifikācijas paaugstināšanos (pieredzes uzkrāšanu) un tehnisko iespēju uzlabošanos (aparatūras un ierīces pilnveidošana) [2, 560].
Endoskopiska asiņošana bija biežākais neveiksmīgas kanulācijas iemesls pre cut papillotomijas gadījumā. Endoskopiski asiņošanas tiek novērotas 10–30 % slimnieku, kam veikta papillotomija, bet tas ne vienmēr liecina par negatīvu iznākumu, jo, piemēram, pacientiem ar mehānisko dzelti asiņošanu parasti saistīja ar traucētu koagulāciju [5, 18].
Pētījuma laikā konstatēts, ka ārstiem ir grūti (nav vienota standarta) noteikt kanulācijas pakāpi. Reizēm pastāv subjektīvs viedoklis, kas ir atkarīgs no endoskopista iepriekšējas pieredzes. Vieglas pakāpes kanulācija ir sastopama visbiežāk. Saskaņā ar pētījuma datiem sarežģītas pakāpes kanulācija visbiežāk ir saistīta ar anatomisku anomāliju, ierobežotu vizualizāciju un individuālu endoskopista pieredzi. Līdz šim brīdim nav stingri definētas kanulācijas sarežģītības pakāpes un nav vienota standarta, taču pasaulē ir piedāvāta Skandināvijas definīcija [7, 248], kas ir universāla un viegli izmantojama. Tās ieviešana palīdz standartizēt procedūras.
Papillotomija bija visbiežākā terapeitiskā procedūra. Salīdzinot PSKUS iepriekšējo pētījumu, pre cut papillotomijas lietošana palielinājās par 2,4 % [3, 1128]. Šo tendenci var saistīt gan ar endoskopistu kvalitātes paaugstināšanos, gan ar izmantoto instrumentu pilnveidošanu.
Procedūras laikā tiek lietotas dažādas terapeitiskās manipulācijas – papillotomija, papillotomija ar žultsakmeņu balona ekstrakciju, papillotomija ar žultsakmeņu groziņa ekstrakciju, papillotomija ar balona ekstrakciju un groziņa ekstrakciju, papillotomija ar žultsvada stenta implantāciju, papillotomija ar d. pancreaticus akmeņu balona ekstrakciju un papillotomija ar d. pancreaticus stenta implantāciju. Šie dati liecina par procedūras izmantošanu dažādos klīniskos gadījumos un dažādām patoloģijām (žultsakmeņu, žultsvada striktūru, aizkuņģa dziedzera un aknu slimību endoskopiskai terapijai) [8, 135].
Saskaņā ar pētījuma datiem agrīnas komplikācijas pēc ERHP procedūras Latvijā ir aktuāla problēma, un, salīdzinot ar literatūras datiem, pētījuma dati atspoguļo labus rezultātus. Literatūras dati par agrīnām komplikācijām pēc ERHP ļoti atšķiras (0,9–12 %) [1, 472; 5, 20; 6, 271]. To varētu izskaidrot ar faktu, ka dažādos gastroenteroloģijas centros tiek dažādi definētas komplikācijas, turklāt atšķiras veikto pētījumu apjoms un endoskopistu pieredze. Komplikāciju definīcijas tiek plaši lietotas kopš 1991. gada, bet ar negatīvu iznākumu saprot arī tehniskās problēmas, procedūras neefektivitāti aktuālās problēmas atrisināšanā, ilglaicīgās sekas, izmaksas, pagarināto hospitalizāciju un pacienta neapmierinātību. Šādā veidā terminoloģija ir attīstījusies no “komplikācijām” uz “blakusparādībām” (angļu val. adverse events) un “neplānotiem notikumiem” (angļu val. unplanned events) [2, 562].
Pētījuma dati liecina, ka visbiežākā komplikācija pēc ERHP ir pankreatīts 2,56 % (4/156) gadījumu ar mirstību – viens pacients (2 mēreni un 2 grūti gadījumi). Vienam pacientam konstatēts holangīts. Literatūras dati rāda, ka antibiotikas profilaktiski var samazināt bakteriēmijas gadījumu skaitu, bet citi – sepses gadījumu skaita samazināšanos pēc ERHP, taču kādā metaanalīzē tika secināts, ka ieguvuma no antibiotiku parakstīšanas nav [1, 473]. Vienam pacientam tika konstatēts miokarda infarkts. Saskaņā ar metaanalīzes datiem (14 prospektīvie pētījumi, 12 973 pacienti) būtiskas kardiopulmonālas komplikācijas ir retas – novēro 1 % gadījumu, un 0,07 % gadījumu tās ir letālas. Komplikācijas iekļauj sirds aritmiju, hipoksēmiju un aspirāciju. Pētījumā, kurā tika salīdzinātas blakusparādības pacientiem, kas vecāki par 65 gadiem, un jaunākiem pacientiem, vecāko pacientu grupā biežāk tika novēroti standarta kardiālie riska faktori, kā arī hemodinamiskas un elektrokardiogrāfiskas izmaiņas, bet šīs izmaiņas nebija statistiski ticamas [4, 22].
Novērošanas laikā nevienam pacientam netika konstatēta asiņošana. Klīniski nozīmīgas asiņošanas, tostarp melēna vai hematemēze, vai arī tās, kas prasa iejaukšanos (endoskopiju vai asins pārliešanu), ir 1–2 % papillotomiju gadījumu. Asiņošana var sākties līdz pat 10 dienu laikā pēc papillotomijas. To novēršanai parasti tiek izmantota endoskopija un ļoti retos gadījumos – ķirurģija. Riska faktori klīniski nozīmīgai asiņošanai ir koagulopātija (tostarp paaugstināts protrombīna laiks, trombocitopēnija vai trombocītu disfunkcija pēc hemodialīzes), antikoagulantās terapijas uzsākšana trīs dienu laikā pēc papillotomijas, endoskopista mazā pieredze [9, 124].
Pēc pētījuma datiem post-ERHP manipulācijas agrīnu komplikāciju izplatība līdzinās citu gastroenteroloģijas klīniku rezultātiem. Pētījums ļāva izvērtēt faktorus, kas ietekmē agrīno komplikāciju attīstību. No visiem analizētajiem faktoriem statistiski ticami ietekmēja tikai vecums (> 65 gadi), normāls bilirubīna līmenis serumā un ķirurģiska iejaukšanās d. pancreaticus, kas korelē ar literatūras datiem [1, 472; 5, 20; 6, 271].
Pētījums parādīja, ka endoskopista pieredze (< 200 procedūru vai > 200 procedūru) statistiski ticami neietekmēja agrīno komplikāciju incidences palielināšanos. Toties A. M. Andersons, analizējot šo faktoru, pierādījis endoskopista ietekmi uz agrīno komplikāciju attīstības risku [1, 469]. Mūsu pētījumā gūtos rezultātus var skaidrot ar nelielo pacientu skaitu.
Ņemot vērā vadlīniju rekomendācijas [6, 273], lai samazinātu PEP incidenci, vienai pacientu grupai pēc procedūras tika ievadīts Supp. Diclofenac natrium 100 mg per rectum. Pētījuma laikā tika pierādīts, ka grupai ar profilaktiskiem pasākumiem PEP izplatība bija mazāka nekā kontrolgrupā (p = 0,045).
Saskaņā ar Eiropas vadlīnijām [6, 275] PEP incidences samazināšanai pacientiem ar augstu risku (pankreatīts pēc iepriekšējās procedūras, vecums > 65 gadi, sieviešu dzimums, normāls bilirubīna līmenis) tika rekomendēta d. pancreaticus profilaktiska stenta implantācija. Stents spontāni evakuējas pēc 5–7 dienām, kad PEP attīstības risks ir minimāls. Šīs manipulācijas, protams, prasa pietiekamu endoskopista pieredzi (vismaz 100 procedūru gadā), procedūras un narkozes laika pagarināšanu, kā arī papildu līdzekļu izmantošanu, tāpēc stentu nerekomendē izmantot visiem pacientiem. Jāpiebilst, ka pēc stenta spontānās evakuācijas papildu manipulācijas nav nepieciešamas.
Lai uzlabotu ERHP rezultātus, galvenie pētījuma virzieni, kuriem būtu jāpievērš uzmanība, ir plašāku datu uzkrāšana, citu Latvijas gastroenteroloģijas centru iesaistīšana datu vākšanā un analīzē, rūpīga pacientu atlase ERHP (atbilstoši indikācijām), d. pancreaticus stenta implantācijas efektivitātes analizēšana, citu riska faktoru padziļināta izpēte. Arī citās gastroenteroloģijas klīnikās regulāri veic prospektīvus pētījumus [3, 1130; 5, 24; 8, 140], lai precizētu agrīnu komplikāciju riska faktorus un nodrošinātu efektīvu profilaksi.
Visām endoskopiskajām procedūrām, it īpaši ERHP, ir raksturīgas komplikācijas. Pārzinot ERHP komplikācijas, to biežumu un riska faktorus, var minimizēt to izplatību un smagumu. Endoskopistiem rūpīgi jāizmeklē pacienti pirms procedūras, jāzina procedūras norise un pieejamās tehnoloģijas un jābūt gataviem novērst komplikācijas. Mirstība un komplikāciju smaguma pakāpe būtiski samazinās, ja komplikācija tiek laikus pamanīta un ātri tiek uzsākta ārstēšana [1, 475]. Komplikāciju pārskats kā daļa no endoskopista izglītības procesa var uzlabot ERHP kvalitāti un nākotnē samazināt komplikāciju attīstības risku.
Ņemot vērā pētījuma rezultātus, pacientiem, kuriem plānota endoskopiska retrogrāda holangiopankreatogrāfija, pēc manipulācijas ieteicams ordinēt Supp. Diclofenac natrium 100 mg, lai samazinātu agrīnu komplikāciju biežumu.
Secinājumi
- Saskaņā ar pētījuma datiem akūts pankreatīts ir biežākā agrīnā komplikācija pēc endoskopiskas retrogrādas holangiopankreatogrāfijas.
- Agrīni komplikāciju attīstības riska faktori ir pacientu vecums, kas lielāks par 65 gadiem, normāls bilirubīna līmenis serumā un ductus pancreaticus kanulācija.
- Supp. Diclofenac natrium lietošana 100 mg devā samazina agrīnu komplikāciju biežumu pēc endoskopiskas retrogrādas holangiopankreatogrāfijas.
Abstract
Endoscopic Retrograde Cholangiopancreatography Short-term Complications Prevalence, Risk Factors and Prevention Possibilities
Endoscopic retrograde cholangiopancreatography (ERCP) is a major therapeutic advance in the management of the pancreatobiliary system diseases. ERCP short-term complications include pancreatitis, haemorrhage and perforation. Reported short-term complication rates vary widely in literature.
The aim of the prospective study was to analyse ERCP cases with emphasis on the overall post-ERCP short-term complication and identification of potential risk factors.
From November 2013 to April 2014, all consecutive ERCP procedures in Pauls Stradiņš University Hospital were included in the study. Patient has data and ERCP related factors entered in a database for further processing and analysis.
Post-ERCP short-term complications developed in 6 of the 156 (9.36 %) patients. Post-ERCP pancreatitis (PEP) was the most common 4/156 (2.56 %) with a mortality rate of 1.56 % (mild and severe and in 2-2 cases). One patient had secondary cholangitis and one – myocardial infarction after ERCP. The results of the analysis showed that older age, normal range of serum bilirubin before ERCP, pancreatic duct injection increased risk of complications independently. Effective PEP prophylaxis has been demonstrated in our study using 100 mg of diclofenac natrium administered rectally (p < 0.045).
ERCP is considered as a low-risk procedure; however, complications can occur. Pancreatitis is the most frequent complication after ERCP with an incidence of 2.5 % patients. Awareness of both patientand procedure-related factors for the development of post-ERCP complication should be considered to stratify patients’ risk.
Literatūra
- Anderson A. M., Fisher L. Complications of ERCP // Gastrointestinal Endoscopy, 2012; 75 (3): 467–475.
- Bai Y., Gao J., Zhang W., et al. Meta-analysis: allopurinol in the prevention of postendoscopic retrograde cholangiopancreatography pancreatitis // Aliment Pharmacology Therapy, 2008; 557–564.
- Chen Y. K., Bai J., Zheng M., et al. Efficacy of diclofenac in the prevention of post-ERCP pancreatitisinpredominantly high-risk patients: a randomized double-blind prospective trial // Gastrointestinal Endoscopy, 2008; 66 (6): 1126–1132.
- Cotton P., Maulsin P., Palesch Y., et al. Pancreatic stenting prevents pancreatitis after biliary sphincterotomy in patients with sphincter of Oddi dysfunction // Gastroenterology, 1998; 115 (15): 18–24.
- Donnellan F., Byrne M. F. Prevention of post-ERCP pancreatitis // Gastroenterology Research and Practice Volume (Article ID 796751), 2012; 1 (1): 12–25.
- Gul H., Yagci G., Simsek A., et al. Beneficial effects of N-acetylcysteine on sodium taurocholate-induced pancreatitis in rats // Journal of Gastroenterology, 2004; 39 (3): 268–276.
- Halttunen J., Søren M. Difficult cannulation as defined by a prospective study of the Scandinavian Association for Digestive Endoscopy (SADE) // ERCPs Scandinavian Journal of Gastroenterology, 2014; 35 (4): 246–249.
- Nishino T., Toki F. Prediction of post-ERCP pancreatitis // Pancreatitis – Treatment and Complications, 2012; 15 (3): 131–144.
- Patel R., Tarnasky P. R., Hawes R. H., et al. Does stenting after pancreatic sphincter- otomy reduce post-ERCP pancreatitis in patients with prior biliary sphincterotomy? Preliminary results of a prospective, randomized trial [abstract] // Gastrointest Endoscopy, 1999; 49 (AB80): 120–127.
- Putnina B., Pukitis A. Results of the treatment of choledocholithiasis using therapeutic endoscopic retrograde holangiopancreatography methods // Pauls Stradins Clinical University Hospital Gastroenterology Centre. Medicine, 2010; 49–60.
- Silvieral M. L., Seamon M. J., Prosciak M. P., et al. Complications related to endoscopic retrograde cholangiopancreatography: A comprehensive clinical review // Journal Gastrointestinal Liver Disorder, 2009; 18 (1): 73–82.
- Shorb P. E., Moscovitz H. Endoscopic cannulation of the ampulla of Vater: a preliminary report // Ann Surg 1968; 167: 752–756.
- Zukens F. J., Hovell D. A., et al. ERCP in the very elderly: outcomes among patients older than eighty // Dig Dis Sci, 2010; 55 (3): 847–851.